समय की शुरुआत के बाद से, मानव ने यह समझने की कोशिश की है कि ब्रह्मांड और उसके भीतर का सब कुछ क्या बना है। और जबकि प्राचीन मागी और दार्शनिकों ने चार या पांच तत्वों से युक्त एक ऐसी दुनिया की कल्पना की थी - पृथ्वी, वायु, जल, अग्नि (और धातु, या चेतना) - शास्त्रीय पुरातनता के द्वारा, दार्शनिक यह सिद्ध करना शुरू कर देते थे कि सभी मामला वास्तव में छोटे से बना है। अदृश्य, और अविभाज्य परमाणु।
उस समय से, वैज्ञानिकों ने परमाणु के साथ चल रही खोज की प्रक्रिया में लगे हुए हैं, जिससे इसकी वास्तविक प्रकृति और श्रृंगार की खोज की उम्मीद है। 20 वीं शताब्दी तक, हमारी समझ इस बिंदु पर परिष्कृत हो गई कि हम इसका एक सटीक मॉडल बनाने में सक्षम थे। और पिछले एक दशक के भीतर, हमारी समझ और भी आगे बढ़ गई है, इस बात के लिए कि हम इसके लगभग सभी पुर्जों के अस्तित्व की पुष्टि कर चुके हैं।
आज, परमाणु अनुसंधान उप-परमाणु स्तर पर संरचना और पदार्थ के कार्य का अध्ययन करने पर केंद्रित है। इसमें न केवल उन सभी उप-परमाणु कणों की पहचान करना शामिल है जिन्हें परमाणु बनाने के लिए सोचा जाता है, बल्कि उन बलों की जांच की जाती है जो उन्हें नियंत्रित करते हैं। इनमें मजबूत परमाणु बल, कमजोर परमाणु बल, विद्युत चुंबकत्व और गुरुत्वाकर्षण शामिल हैं। यहाँ अब तक परमाणु के बारे में जानने के लिए हम सभी का एक टूटना है ...
परमाणु की संरचना:
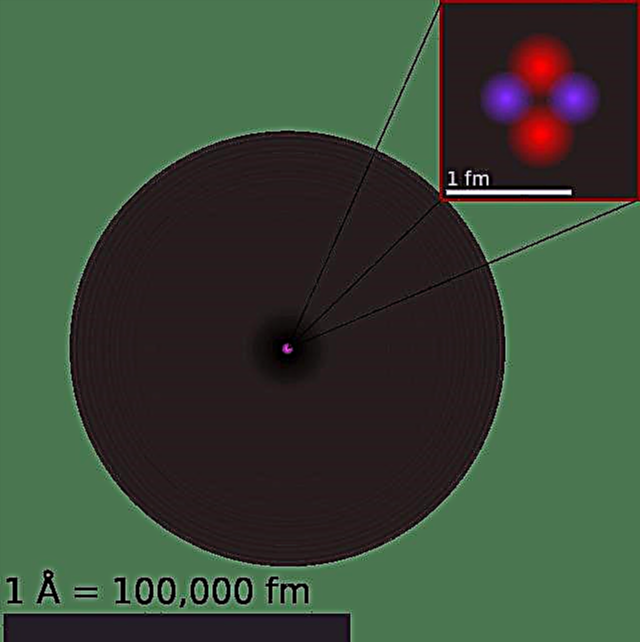
परमाणु के हमारे वर्तमान मॉडल को तीन घटक भागों - प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों में विभाजित किया जा सकता है। इन भागों में से प्रत्येक में एक संबद्ध चार्ज होता है, जिसमें प्रोटॉन एक सकारात्मक चार्ज होता है, इलेक्ट्रॉनों का ऋणात्मक आवेश होता है और न्यूट्रॉन का शुद्ध आवेश होता है। कण भौतिकी के मानक मॉडल के अनुसार, प्रोटॉन और न्यूट्रॉन परमाणु के नाभिक का निर्माण करते हैं, जबकि इलेक्ट्रॉन इसे "क्लाउड" में परिक्रमा करते हैं।

एक परमाणु में इलेक्ट्रॉनों को विद्युत चुम्बकीय बल द्वारा नाभिक में प्रोटॉन के लिए आकर्षित किया जाता है। इलेक्ट्रॉन अपनी कक्षा से बच सकते हैं, लेकिन केवल ऊर्जा के एक बाहरी स्रोत के जवाब में। नाभिक के लिए इलेक्ट्रॉन की करीब कक्षा, अधिक आकर्षक बल; इसलिए, बाहरी बल को एक इलेक्ट्रॉन को बच निकलने के लिए आवश्यक था।
इलेक्ट्रॉन नाभिक की कई कक्षाओं में परिक्रमा करते हैं, जिनमें से प्रत्येक इलेक्ट्रॉन के एक विशेष ऊर्जा स्तर से मेल खाता है। इलेक्ट्रॉन अपने राज्य को एक उच्च ऊर्जा स्तर में बदल सकता है, जिससे एक फोटॉन को पर्याप्त ऊर्जा के साथ अवशोषित करके नए क्वांटम राज्य में बढ़ाया जा सके। इसी तरह, एक उच्च ऊर्जा राज्य में एक इलेक्ट्रॉन एक कम ऊर्जा राज्य के लिए एक फोटॉन के रूप में अतिरिक्त ऊर्जा विकीर्ण कर सकते हैं।
यदि परमाणु समान रूप से प्रोटॉन और इलेक्ट्रॉनों की संख्या के साथ परमाणु तटस्थ हैं। जिन परमाणुओं में इलेक्ट्रॉनों की कमी या अधिशेष है, उन्हें आयन कहा जाता है। इलेक्ट्रॉनों जो नाभिक से सबसे दूर होते हैं, उन्हें पास के अन्य परमाणुओं में स्थानांतरित किया जा सकता है या परमाणुओं के बीच साझा किया जा सकता है। इस तंत्र द्वारा, परमाणु अणुओं और अन्य प्रकार के रासायनिक यौगिकों में बंधने में सक्षम होते हैं।
इन सभी उप-परमाणु कणों में से एक है, पदार्थ से जुड़े कण का एक वर्ग, जो प्रकृति में प्राथमिक (इलेक्ट्रॉनों) या समग्र (प्रोटॉन और न्यूट्रॉन) है। इसका मतलब है कि इलेक्ट्रॉनों की कोई आंतरिक संरचना नहीं है, जबकि प्रोटॉन और न्यूट्रॉन अन्य उप-परमाणु कणों से बने होते हैं। क्वार्क कहा जाता है। परमाणुओं में दो प्रकार के क्वार्क होते हैं, जिनमें एक भिन्नात्मक विद्युत आवेश होता है।

प्रोटॉन दो "अप" क्वार्क से मिलकर बने होते हैं (प्रत्येक में +2/3 का चार्ज होता है) और एक "डाउन" क्वार्क (-1/3), जबकि न्यूट्रॉन में एक क्वार्क और दो डाउन क्वार्क होते हैं। यह अंतर दो कणों के बीच प्रभारी के अंतर के लिए होता है, जो क्रमशः +1 और 0 के चार्ज के लिए काम करता है, जबकि इलेक्ट्रॉनों में -1 का चार्ज होता है।
अन्य उप-परमाणु कणों में लेप्टोन शामिल हैं, जो पदार्थ के निर्माण खंडों को बनाने के लिए फर्मन्स के साथ संयोजन करते हैं। वर्तमान परमाणु मॉडल में छह लेप्टान हैं: इलेक्ट्रॉन, म्यूऑन और ताऊ कण और उनके संबंधित न्यूट्रिनो। लेप्टान कणों की विभिन्न किस्मों, जिन्हें आमतौर पर "फ्लेवर" कहा जाता है, उनके आकार और आवेशों द्वारा विभेदित होते हैं, जो उनके विद्युत चुम्बकीय इंटरैक्शन के स्तर को प्रभावित करते हैं।
इसके बाद, गेज बॉसन हैं, जिन्हें "बल वाहक" के रूप में जाना जाता है क्योंकि वे शारीरिक बलों की मध्यस्थता करते हैं। उदाहरण के लिए, ग्लूऑन मजबूत परमाणु बल के लिए ज़िम्मेदार होते हैं जो एक साथ क्वार्कों को धारण करते हैं जबकि डब्ल्यू और जेड बोसॉन (अभी भी काल्पनिक) को विद्युत चुंबकत्व के पीछे कमजोर परमाणु बल के लिए जिम्मेदार माना जाता है। फोटोन प्राथमिक कण है जो प्रकाश बनाता है, जबकि हिग्स बोसोन डब्ल्यू और जेड बोसोन को उनके द्रव्यमान देने के लिए जिम्मेदार है।
परमाणु भार:
एक परमाणु द्रव्यमान का अधिकांश भाग प्रोटॉन और न्यूट्रॉन से आता है जो इसके नाभिक का निर्माण करते हैं। इलेक्ट्रॉन एक परमाणु के घटक कणों में से सबसे कम बड़े पैमाने पर होते हैं, जिसमें 9.11 x 10 का द्रव्यमान होता है-31 किलो और एक आकार वर्तमान तकनीकों द्वारा मापा जा सकता है। प्रोटॉन का द्रव्यमान 1,836 गुना होता है जो कि इलेक्ट्रॉन का 1.6726 × 10 होता है-27 किग्रा, जबकि न्यूट्रॉन तीनों में सबसे बड़े हैं, 1.6929 × 10 पर-27 किग्रा (इलेक्ट्रॉन के द्रव्यमान का 1,839 गुना)।

एक परमाणु के नाभिक में प्रोटॉन और न्यूट्रॉन की कुल संख्या ("नाभिक" कहा जाता है) को जन संख्या कहा जाता है। उदाहरण के लिए, तत्व कार्बन -12 को इसलिए नाम दिया गया है क्योंकि इसकी 12 न्यूक्लियनों (छह प्रोटॉन और छह न्यूट्रॉन) से व्युत्पन्न 12 की एक बड़ी संख्या है। हालांकि, तत्वों को उनके परमाणु संख्या के आधार पर भी व्यवस्थित किया जाता है, जो नाभिक में पाए जाने वाले प्रोटॉन की संख्या के समान है। इस मामले में, कार्बन की परमाणु संख्या 6 है।
आराम से एक परमाणु का वास्तविक द्रव्यमान मापना बहुत मुश्किल है, क्योंकि पारंपरिक इकाइयों में व्यक्त करने के लिए परमाणुओं का सबसे अधिक भारी भी हल्का होता है। जैसे, वैज्ञानिक अक्सर एकीकृत परमाणु द्रव्यमान इकाई (यू) का उपयोग करते हैं - जिसे डाल्टन (दा) भी कहा जाता है - जिसे कार्बन के मुक्त तटस्थ परमाणु के द्रव्यमान के बारहवें के रूप में परिभाषित किया गया है, जो लगभग 1.66 × 10 है-27 किलोग्राम।
रसायनज्ञ भी मोल्स का उपयोग करते हैं, एक इकाई जिसे किसी भी तत्व के एक मोल के रूप में परिभाषित किया जाता है जिसमें हमेशा परमाणुओं की संख्या होती है (लगभग 6.022 × 10)23)। यह संख्या इसलिए चुनी गई थी कि यदि किसी तत्व का परमाणु भार 1 u है, तो उस तत्व के परमाणुओं का एक द्रव्यमान एक ग्राम के करीब होता है। एकीकृत परमाणु द्रव्यमान इकाई की परिभाषा के कारण, प्रत्येक कार्बन -12 परमाणु का परमाणु द्रव्यमान ठीक 12 u है, और इसलिए कार्बन -12 परमाणुओं के एक तिल का वजन ठीक 0.012 किलोग्राम है।
रेडियोधर्मी क्षय:
प्रोटॉन की जितनी भी दो परमाणु संख्याएँ हैं, वे एक ही रासायनिक तत्व के हैं। लेकिन प्रोटॉन की समान संख्या वाले परमाणुओं में एक अलग संख्या में न्यूट्रॉन हो सकते हैं, जिन्हें एक ही तत्व के अलग-अलग समस्थानिक के रूप में परिभाषित किया जाता है। ये समस्थानिक अक्सर अस्थिर होते हैं, और 82 से अधिक परमाणु संख्या वाले सभी लोग रेडियोधर्मी होते हैं।
जब कोई तत्व क्षय करता है, तो उसका नाभिक विकिरण उत्सर्जित करके ऊर्जा खो देता है - जिसमें अल्फा कण (हीलियम परमाणु), बीटा कण (पॉज़िट्रॉन), गामा किरणें (उच्च-आवृत्ति विद्युत चुम्बकीय ऊर्जा) और रूपांतरण इलेक्ट्रॉन शामिल हो सकते हैं। जिस दर पर एक अस्थिर तत्व का क्षय होता है, उसे "अर्ध-जीवन" के रूप में जाना जाता है, जो तत्व के प्रारंभिक मूल्य के आधे पर गिरने के लिए आवश्यक समय की मात्रा है।
एक आइसोटोप की स्थिरता न्यूट्रॉन के प्रोटॉन के अनुपात से प्रभावित होती है। पृथ्वी पर स्वाभाविक रूप से पाए जाने वाले 339 विभिन्न प्रकार के तत्वों में से 254 (लगभग 75%) को "स्थिर आइसोटोप" के रूप में लेबल किया गया है - अर्थात् क्षय के अधीन नहीं। एक अतिरिक्त 34 रेडियोधर्मी तत्वों में 80 मिलियन वर्षों से अधिक का आधा जीवन होता है, और प्रारंभिक सौर प्रणाली के बाद से अस्तित्व में भी है (इसलिए उन्हें "आदिम तत्व" कहा जाता है)।
अंत में, एक अतिरिक्त 51 अल्पकालिक तत्वों को स्वाभाविक रूप से "बेटी तत्वों" (यानी परमाणु उप-उत्पादों) के रूप में जाना जाता है, जो अन्य तत्वों के क्षय (जैसे यूरेनियम से रेडियम) के रूप में होते हैं। इसके अलावा, अल्पकालिक रेडियोधर्मी तत्व पृथ्वी पर प्राकृतिक ऊर्जावान प्रक्रियाओं का परिणाम हो सकते हैं, जैसे कि ब्रह्मांडीय किरण बमबारी (उदाहरण के लिए, कार्बन -14, जो हमारे वायुमंडल में होता है)।
अध्ययन का इतिहास:
परमाणु सिद्धांत का सबसे पहला ज्ञात उदाहरण प्राचीन ग्रीस और भारत से आता है, जहाँ डेमोक्रिटस जैसे दार्शनिकों ने माना कि यह सारा मामला छोटी, अविभाज्य और अविनाशी इकाइयों से बना था। शब्द "परमाणु" प्राचीन ग्रीस में गढ़ा गया था और "परमाणुवाद" के रूप में जाना जाने वाले विचार के स्कूल को जन्म दिया। हालाँकि, यह सिद्धांत एक वैज्ञानिक की तुलना में दार्शनिक अवधारणा से अधिक था।
यह 19 वीं शताब्दी तक नहीं था कि परमाणुओं के सिद्धांत को एक वैज्ञानिक पदार्थ के रूप में व्यक्त किया गया था, पहले साक्ष्य-आधारित प्रयोगों का संचालन किया गया था। उदाहरण के लिए, 1800 के शुरुआती दिनों में, अंग्रेजी वैज्ञानिक जॉन डाल्टन ने परमाणु की अवधारणा का उपयोग यह समझाने के लिए किया था कि रासायनिक तत्वों ने कुछ अवलोकन योग्य और अनुमानित तरीकों से प्रतिक्रिया क्यों की।
डाल्टन ने इस सवाल के साथ शुरू किया कि तत्वों ने छोटी संख्याओं के अनुपात में प्रतिक्रिया क्यों की, और निष्कर्ष निकाला कि ये प्रतिक्रियाएं पूरी संख्या में असतत इकाइयों के गुणकों में हुई हैं - दूसरे शब्दों में, परमाणु। गैसों से जुड़े प्रयोगों की एक श्रृंखला के माध्यम से, डाल्टन को विकसित किया गया जिसे डाल्टन के परमाणु सिद्धांत के रूप में जाना जाता है, जो आधुनिक भौतिकी और रसायन विज्ञान के कोने में से एक है।
सिद्धांत पांच परिसरों में नीचे आता है: तत्व, उनकी शुद्धतम स्थिति में, परमाणुओं नामक कणों से मिलकर बनता है; एक विशिष्ट तत्व के परमाणु सभी समान हैं, बहुत आखिरी परमाणु के नीचे; विभिन्न तत्वों के परमाणुओं को उनके परमाणु भार से अलग बताया जा सकता है; तत्वों के परमाणु रासायनिक यौगिकों को बनाने के लिए एकजुट होते हैं; रासायनिक प्रतिक्रिया में परमाणुओं को न तो बनाया जा सकता है और न ही नष्ट किया जा सकता है, केवल समूह कभी बदलता है।
19 वीं शताब्दी के अंत तक, वैज्ञानिकों ने यह सिद्ध करना शुरू कर दिया कि परमाणु एक से अधिक मौलिक इकाई से बना है। हालांकि, अधिकांश वैज्ञानिकों ने कहा कि यह इकाई सबसे छोटे ज्ञात परमाणु - हाइड्रोजन के आकार की होगी। और फिर 1897 में, कैथोड किरणों का उपयोग करते हुए प्रयोगों की एक श्रृंखला के माध्यम से, भौतिक विज्ञानी जे.जे. थॉम्पसन ने घोषणा की कि उन्होंने एक ऐसी इकाई की खोज की है जो हाइड्रोजन परमाणु की तुलना में 1000 गुना छोटी और 1800 गुना हल्की थी।

उनके प्रयोगों से यह भी पता चला कि वे फोटोइलेक्ट्रिक प्रभाव और रेडियोधर्मी पदार्थों द्वारा बंद कणों के समान थे। बाद के प्रयोगों से पता चला कि यह कण धातु के तारों और परमाणुओं के भीतर नकारात्मक विद्युत आवेशों के माध्यम से विद्युत प्रवाह करता है। इसलिए कण - जिसे मूल रूप से "कॉर्पसकल" नाम दिया गया था - बाद में कण जॉर्ज जॉन्सन स्टोइन के 1874 में पूर्वानुमानित होने के बाद, इसे "इलेक्ट्रॉन" में बदल दिया गया।
हालांकि, थॉमसन ने यह भी कहा कि इलेक्ट्रॉनों को पूरे परमाणु में वितरित किया गया था, जो सकारात्मक चार्ज का एक समान समुद्र था। इसे "प्लम पुडिंग मॉडल" के रूप में जाना जाता है, जिसे बाद में गलत साबित किया जाएगा। यह 1909 में हुआ था, जब भौतिक विज्ञानी हंस गिगर और अर्नेस्ट मार्सडेन (अर्नेस्ट रदरफोड के निर्देशन में) ने धातु के पन्नी और अल्फा कणों का उपयोग करके अपना प्रयोग किया था।
डाल्टन के परमाणु मॉडल के अनुरूप, उनका मानना था कि अल्फा कण थोड़ा विक्षेपण के साथ सीधे पन्नी से गुजरेंगे। हालांकि, कई कणों को 90 ° से अधिक कोणों पर विक्षेपित किया गया था। यह समझाने के लिए, रदरफोर्ड ने प्रस्ताव दिया कि परमाणु का सकारात्मक चार्ज केंद्र में एक छोटे से नाभिक में केंद्रित है।
1913 में, भौतिक विज्ञानी नील्स बोह्र ने एक मॉडल का प्रस्ताव रखा जहां इलेक्ट्रॉनों ने नाभिक की परिक्रमा की, लेकिन कक्षाओं के एक सीमित सेट में ही ऐसा कर सकते थे। उन्होंने यह भी प्रस्तावित किया कि इलेक्ट्रॉन कक्षाओं के बीच कूद सकते हैं, लेकिन केवल एक फोटॉन के अवशोषण या विकिरण के अनुरूप ऊर्जा के असतत परिवर्तनों में। इसने न केवल रदरफोर्ड के प्रस्तावित मॉडल को परिष्कृत किया, बल्कि एक मात्रा वाले परमाणु की अवधारणा को भी जन्म दिया, जहां विचारशील पैकेट में व्यवहार किया गया।

द्रव्यमान स्पेक्ट्रोमीटर का विकास - जो आयनों के एक किरण के प्रक्षेपवक्र को मोड़ने के लिए एक चुंबक का उपयोग करता है - परमाणुओं के द्रव्यमान को बढ़ी हुई सटीकता के साथ मापने की अनुमति दी। केमिस्ट फ्रांसिस विलियम एस्टन ने इस उपकरण का इस्तेमाल यह दिखाने के लिए किया कि आइसोटोप में अलग-अलग द्रव्यमान होते हैं। इसके बाद भौतिक विज्ञानी जेम्स चैडविक ने इसका अनुसरण किया, जिन्होंने 1932 में न्यूट्रॉन को आइसोटोप के अस्तित्व को समझाने के एक तरीके के रूप में प्रस्तावित किया था।
20 वीं शताब्दी की शुरुआत में, परमाणुओं की क्वांटम प्रकृति को और विकसित किया गया था। 1922 में, जर्मन भौतिकविदों ओटो स्टर्न और वाल्थर गेर्लच ने एक प्रयोग किया, जिसमें एक चुंबकीय क्षेत्र के माध्यम से चांदी के परमाणुओं के एक बीम को निर्देशित किया गया था, जिसका उद्देश्य परमाणुओं कोणीय गति (या स्पिन) की दिशा के बीच बीम को विभाजित करना था।
स्टर्न-गेरलच प्रयोग के रूप में जाना जाता है, परिणाम यह था कि बीम के दो हिस्सों को विभाजित किया गया था, इस पर निर्भर करता है कि परमाणुओं का स्पिन ऊपर या नीचे उन्मुख था या नहीं। 1926 में, भौतिक विज्ञानी एरविन श्रोडिंगर ने एक गणितीय मॉडल को विकसित करने के लिए तरंगों की तरह व्यवहार करने वाले कणों के विचार का इस्तेमाल किया, जिन्होंने इलेक्ट्रॉनों को मात्र कणों के बजाय तीन-आयामी तरंगों के रूप में वर्णित किया।
कणों का वर्णन करने के लिए तरंगों का उपयोग करने का एक परिणाम यह है कि किसी भी समय किसी कण की स्थिति और गति दोनों के लिए सटीक मान प्राप्त करना गणितीय रूप से असंभव है। उसी वर्ष, वर्नर हाइजेनबर्ग ने इस समस्या को तैयार किया और इसे "अनिश्चितता सिद्धांत" कहा। हेइज़ेनबर्ग के अनुसार, स्थिति के दिए गए सटीक माप के लिए, कोई केवल गति के लिए संभावित मूल्यों की एक श्रृंखला प्राप्त कर सकता है, और इसके विपरीत।

1930 के दशक में, भौतिकविदों ने परमाणु विखंडन की खोज की, जो ओटो हैन, लिस मितनर और ओटो फ्रिस्क के प्रयोगों के लिए धन्यवाद था। हुरन के प्रयोगों में एक यूरेनियम परमाणुओं पर एक न्यूट्रानियम तत्व बनाने की उम्मीद में न्यूट्रॉन को निर्देशित करना शामिल था। इसके बजाय, प्रक्रिया ने यूरेनियम -92 (यूआर) का अपना नमूना बदल दिया92) दो नए तत्वों में - बेरियम (बी)56) और क्रिप्टन (क्र27).
Meitner और Frisch ने प्रयोग का सत्यापन किया और इसे यूरेनियम परमाणुओं में विभाजित करके दो तत्वों को एक ही कुल परमाणु भार के साथ विभाजित करने के लिए जिम्मेदार ठहराया, एक प्रक्रिया जिसने परमाणु बांडों को तोड़कर काफी मात्रा में ऊर्जा भी जारी की। इसके बाद के वर्षों में, इस प्रक्रिया के संभावित हथियारीकरण (यानी परमाणु हथियार) पर शोध शुरू हुआ और 1945 तक अमेरिका में पहले परमाणु बमों के निर्माण का नेतृत्व किया गया।
1950 के दशक में, बेहतर कण त्वरक और कण डिटेक्टरों के विकास ने वैज्ञानिकों को उच्च ऊर्जा पर चलने वाले परमाणुओं के प्रभावों का अध्ययन करने की अनुमति दी। इससे कण भौतिकी का मानक मॉडल विकसित किया गया था, जो अब तक नाभिक के गुणों, प्रमेयकृत उप-परमाणु कणों के अस्तित्व और उनकी अंतःक्रियाओं को नियंत्रित करने वाली शक्तियों को सफलतापूर्वक समझा चुका है।
आधुनिक प्रयोग:
20 वीं शताब्दी के उत्तरार्ध के बाद से, कई नए और रोमांचक खोज परमाणु सिद्धांत और क्वांटम यांत्रिकी के संबंध में रहे हैं। उदाहरण के लिए, 2012 में, हिग्स बोसोन की लंबी खोज ने एक सफलता हासिल की, जहां स्विट्जरलैंड में यूरोपीय संगठन परमाणु अनुसंधान (सर्न) में काम करने वाले शोधकर्ताओं ने इसकी खोज की घोषणा की।

हाल के दशकों में, भौतिकविदों द्वारा एक एकीकृत क्षेत्र सिद्धांत (उर्फ ग्रैंड यूनिफाइंग थ्योरी या थ्योरी ऑफ एवरीथिंग) के विकास के लिए समय और ऊर्जा का एक बड़ा सौदा समर्पित किया गया है। संक्षेप में, चूंकि स्टैंडर्ड मॉडल पहली बार प्रस्तावित किया गया था, वैज्ञानिकों ने यह समझने की कोशिश की है कि ब्रह्मांड के चार मूलभूत बल (गुरुत्वाकर्षण, मजबूत और कमजोर परमाणु बल और विद्युत चुंबकत्व) एक साथ कैसे काम करते हैं।
जबकि आइंस्टीन के सापेक्षता के सिद्धांतों का उपयोग करके गुरुत्वाकर्षण को समझा जा सकता है, और परमाणु बलों और विद्युत चुंबकत्व को क्वांटम सिद्धांत का उपयोग करके समझा जा सकता है, न ही सिद्धांत एक साथ काम करने वाले सभी चार बलों के लिए जिम्मेदार हो सकता है। इसे हल करने के प्रयासों ने वर्षों में कई प्रस्तावित सिद्धांतों को जन्म दिया है, जिसमें स्ट्रिंग थ्योरी से लेकर लूप क्वांटम ग्रेविटी तक शामिल हैं। आज तक, इनमें से किसी भी सिद्धांत ने सफलता नहीं पाई है।
परमाणु की हमारी समझ एक लंबा रास्ता तय कर चुकी है, शास्त्रीय मॉडलों से जिसने इसे एक जड़ ठोस के रूप में देखा था जो अन्य परमाणुओं के साथ यंत्रवत् रूप से बातचीत करता था, आधुनिक सिद्धांतों के लिए जहां परमाणु ऊर्जावान कणों से बने होते हैं जो अप्रत्याशित व्यवहार करते हैं। जबकि इसे कई हजार साल हो गए हैं, सभी मामलों की बुनियादी संरचना के बारे में हमारा ज्ञान काफी उन्नत हो चुका है।
और फिर भी, कई रहस्य बने हुए हैं जिनका समाधान होना बाकी है। समय और निरंतर प्रयासों के साथ, हम अंत में परमाणु के अंतिम शेष रहस्यों को अनलॉक कर सकते हैं। तो फिर, यह बहुत अच्छी तरह से हो सकता है कि हम जो भी नई खोज करेंगे वह केवल और अधिक प्रश्नों को जन्म देगा - और वे पहले की तुलना में कहीं अधिक भ्रमित हो सकते हैं!
हमने अंतरिक्ष पत्रिका के परमाणु के बारे में कई लेख लिखे हैं। यहाँ जॉन डाल्टन के परमाणु मॉडल, नील बोहर के परमाणु मॉडल, हू डेमोक्रेसीएटी के बारे में एक लेख है?, और ब्रह्मांड में कितने परमाणु हैं?
यदि आप परमाणु के बारे में अधिक जानकारी चाहते हैं, तो छोटे नमूनों का विश्लेषण करने पर नासा के लेख की जाँच करें, और यहाँ परमाणुओं, तत्वों और आइसोटोप के बारे में नासा के लेख का लिंक दिया गया है।
हमने एटम के बारे में खगोल विज्ञान कास्ट का एक संपूर्ण प्रकरण भी दर्ज किया है। यहां सुनें, एपिसोड 164: इनसाइड द एटम, एपिसोड 263: रेडियोधर्मी क्षय, और एपिसोड 394: द स्टैंडर्ड मॉडल, बॉसन।