20 वीं सदी की शुरुआत में विज्ञान के लिए एक बहुत ही शुभ समय था। अर्नेस्ट रदरफोर्ड और नील्स बोह्र के अलावा कण भौतिकी के मानक मॉडल को जन्म देते हुए, यह क्वांटम यांत्रिकी के क्षेत्र में सफलताओं का एक दौर था। इलेक्ट्रॉनों के व्यवहार पर चल रहे अध्ययनों के लिए धन्यवाद, वैज्ञानिकों ने सिद्धांतों का प्रस्ताव करना शुरू किया जिससे इन प्राथमिक कणों ने शास्त्रीय, न्यूटोनियन भौतिकी को परिभाषित करने वाले तरीकों का व्यवहार किया।
ऐसा ही एक उदाहरण इर्विन श्रोडिंगर द्वारा प्रस्तावित इलेक्ट्रॉन क्लाउड मॉडल है। इस मॉडल के लिए धन्यवाद, इलेक्ट्रॉनों को एक निश्चित कक्षा में केंद्रीय नाभिक के चारों ओर घूमने वाले कणों के रूप में नहीं दिखाया गया था। इसके बजाय, श्रोडिंगर ने एक मॉडल का प्रस्ताव रखा जिसके तहत वैज्ञानिक केवल इलेक्ट्रॉनों के पदों के रूप में शिक्षित अनुमान लगा सकते थे। इसलिए, उनके स्थानों को केवल नाभिक के चारों ओर एक 'क्लाउड' का हिस्सा बताया जा सकता है जहां इलेक्ट्रॉनों के पाए जाने की संभावना है।
20 वीं शताब्दी में परमाणु भौतिकी:
परमाणु सिद्धांत का सबसे पहला ज्ञात उदाहरण प्राचीन ग्रीस और भारत से आता है, जहां डेमोक्रिटस जैसे दार्शनिकों ने माना कि यह सारा मामला छोटी, अविभाज्य और अविनाशी इकाइयों से बना था। शब्द "परमाणु" प्राचीन ग्रीस में गढ़ा गया था और "परमाणुवाद" के रूप में जाना जाने वाले विचार के स्कूल को जन्म दिया। हालाँकि, यह सिद्धांत एक वैज्ञानिक की तुलना में दार्शनिक अवधारणा से अधिक था।
यह 19 वीं शताब्दी तक नहीं था कि परमाणुओं के सिद्धांत को एक वैज्ञानिक पदार्थ के रूप में व्यक्त किया गया था, पहले साक्ष्य-आधारित प्रयोगों का संचालन किया गया था। उदाहरण के लिए, 1800 के शुरुआती दिनों में, अंग्रेजी वैज्ञानिक जॉन डाल्टन ने परमाणु की अवधारणा का उपयोग यह समझाने के लिए किया था कि रासायनिक तत्वों ने कुछ अवलोकन योग्य और अनुमानित तरीकों से प्रतिक्रिया क्यों की। गैसों से संबंधित प्रयोगों की एक श्रृंखला के माध्यम से, डाल्टन को विकसित करने के लिए चला गया जिसे डाल्टन के परमाणु सिद्धांत के रूप में जाना जाता है।
यह सिद्धांत बड़े पैमाने पर और निश्चित अनुपात की बातचीत के कानूनों पर विस्तारित हुआ और पांच परिसरों तक नीचे आया: तत्वों, उनकी शुद्धतम स्थिति में, परमाणुओं नामक कणों से मिलकर; एक विशिष्ट तत्व के परमाणु सभी समान हैं, बहुत आखिरी परमाणु के नीचे; विभिन्न तत्वों के परमाणुओं को उनके परमाणु भार से अलग बताया जा सकता है; तत्वों के परमाणु रासायनिक यौगिकों को बनाने के लिए एकजुट होते हैं; रासायनिक प्रतिक्रिया में परमाणुओं को न तो बनाया जा सकता है और न ही नष्ट किया जा सकता है, केवल समूह कभी बदलता है।
इलेक्ट्रॉन की खोज:
19 वीं शताब्दी के अंत तक, वैज्ञानिकों ने यह भी सिद्ध करना शुरू कर दिया कि परमाणु एक से अधिक मौलिक इकाई से बना है। हालांकि, अधिकांश वैज्ञानिकों ने कहा कि यह इकाई सबसे छोटे ज्ञात परमाणु - हाइड्रोजन के आकार की होगी। 19 वीं सदी के अंत तक, सर जोसेफ जॉन थॉमसन जैसे वैज्ञानिकों द्वारा किए गए शोध के कारण, उनका स्वभाव काफी बदल गया।
कैथोड रे ट्यूब (क्रोकस ट्यूब के रूप में जाना जाता है) का उपयोग करने की एक श्रृंखला के माध्यम से, थॉमसन ने देखा कि कैथोड किरणों को विद्युत और चुंबकीय क्षेत्रों द्वारा विक्षेपित किया जा सकता है। उन्होंने निष्कर्ष निकाला कि प्रकाश से बना होने के बजाय, वे नकारात्मक रूप से आवेशित कणों से बने थे जो हाइड्रोजन से 1ooo गुना छोटे और 1800 गुना हल्के थे।

इसने इस धारणा को प्रभावी ढंग से खारिज कर दिया कि हाइड्रोजन परमाणु पदार्थ की सबसे छोटी इकाई थी, और थॉम्पसन यह बताने के लिए आगे बढ़े कि परमाणु अदृश्य थे। परमाणु के समग्र प्रभार की व्याख्या करने के लिए, जिसमें सकारात्मक और नकारात्मक दोनों आरोप शामिल थे, थॉम्पसन ने एक मॉडल का प्रस्ताव दिया, जिसके द्वारा नकारात्मक चार्ज किए गए "कॉर्पसुडर" को सकारात्मक चार्ज के एक समान समुद्र में वितरित किया गया - जिसे प्लम पुडिंग मॉडल के रूप में जाना जाता है।
1874 में एंग्लो-आयरिश भौतिक विज्ञानी जॉर्ज जॉनस्टोन स्टोनी द्वारा भविष्यवाणी की गई सैद्धांतिक कण के आधार पर इन शवों को बाद में "इलेक्ट्रॉन्स" नाम दिया जाएगा। और इससे प्लम पुडिंग मॉडल का जन्म हुआ, इसलिए इसका नामकरण इसलिए किया गया क्योंकि यह अंग्रेजी रेगिस्तान से मिलकर बना था। बेर केक और किशमिश। अवधारणा को यूके के मार्च 1904 संस्करण में दुनिया के सामने पेश किया गया था दार्शनिक पत्रिका, व्यापक प्रशंसा के लिए।
मानक मॉडल का विकास:
बाद के प्रयोगों से प्लम पुडिंग मॉडल के साथ कई वैज्ञानिक समस्याएं सामने आईं। शुरुआत के लिए, यह प्रदर्शित करने की समस्या थी कि परमाणु के पास एक समान सकारात्मक पृष्ठभूमि चार्ज था, जिसे "थॉमसन समस्या" के रूप में जाना जाता था। पांच साल बाद, मॉडल को हंस गेइगर और अर्नेस्ट मार्सडेन द्वारा अस्वीकृत किया जाएगा, जिन्होंने अल्फा कणों और सोने की पन्नी - उर्फ का उपयोग करके कई प्रयोग किए। "गोल्ड फ़ॉइल प्रयोग।"
इस प्रयोग में, Geiger और Marsden ने फ्लोरोसेंट स्क्रीन के साथ अल्फा कणों के बिखरने वाले पैटर्न को मापा। यदि थॉमसन का मॉडल सही था, तो अल्फा कण बिना पन्नी वाले परमाणु संरचना से गुजरेंगे। हालांकि, उन्होंने इसके बजाय यह नोट किया कि अधिकांश शॉट सीधे होते हुए, उनमें से कुछ विभिन्न दिशाओं में बिखरे हुए थे, कुछ स्रोत की दिशा में वापस जा रहे थे।

गीजर और मार्सडेन ने निष्कर्ष निकाला कि कणों को थोमसन के मॉडल द्वारा अनुमति की तुलना में कहीं अधिक इलेक्ट्रोस्टैटिक बल का सामना करना पड़ा। चूँकि अल्फा कण सिर्फ हीलियम नाभिक (जो धनात्मक रूप से आवेशित होते हैं) इस का तात्पर्य है कि परमाणु में धनात्मक आवेश व्यापक रूप से फैलाया नहीं गया था, बल्कि एक छोटी मात्रा में केंद्रित था। इसके अलावा, इस तथ्य को कि जिन कणों को विक्षेपित नहीं किया गया था, वे निर्बाध से गुजरते थे, इसका मतलब था कि ये सकारात्मक रिक्त स्थान खाली जगह के विशाल हिस्से से अलग हो गए थे।
1911 तक भौतिक विज्ञानी अर्नेस्ट रदरफोर्ड ने गीजर-मार्सडेन प्रयोगों की व्याख्या की और थॉमसन के परमाणु मॉडल को खारिज कर दिया। इसके बजाय, उन्होंने एक मॉडल का प्रस्ताव रखा जहां परमाणु में ज्यादातर खाली जगह होती थी, जिसके सभी सकारात्मक चार्ज उसके केंद्र में बहुत कम मात्रा में केंद्रित होते थे, जो इलेक्ट्रॉनों के बादल से घिरा हुआ था। यह परमाणु के रदरफोर्ड मॉडल के रूप में जाना जाता है।
एंटोनियस वैन डेन ब्रोक और नील्स बोह्र द्वारा बाद के प्रयोगों ने मॉडल को और परिष्कृत किया। जबकि वैन डेन ब्रोके ने सुझाव दिया कि किसी तत्व की परमाणु संख्या उसके परमाणु आवेश के समान होती है, बाद वाले ने परमाणु का एक सौर-प्रणाली जैसा मॉडल प्रस्तावित किया, जहां एक नाभिक में परमाणु का धनात्मक आवेश होता है और वह एक बराबर से घिरा होता है। कक्षीय गोले (उर्फ। बोहर मॉडल) में इलेक्ट्रॉनों की संख्या।
इलेक्ट्रॉन क्लाउड मॉडल:
1920 के दशक के दौरान, ऑस्ट्रियाई भौतिक विज्ञानी एरविन श्रोडिंगर थ्योरी मैक्स प्लैंक, अल्बर्ट आइंस्टीन, नील्स बोहर, अर्नोल्ड सोमरफेल्ड, और अन्य भौतिकविदों से मोहित हो गए। इस समय के दौरान, वह परमाणु सिद्धांत और स्पेक्ट्रा के क्षेत्रों में भी शामिल हो गए, उन्होंने ज्यूरिख विश्वविद्यालय और फिर बर्लिन में फ्रेडरिक विल्हेम विश्वविद्यालय (जहां वे 1927 में प्लांक में सफल हुए) पर शोध किया।

1926 में, श्रोडिंगर ने लहरों के कार्यों और इलेक्ट्रॉनों की समस्याओं को हल किया। यह वर्णन करने के अलावा कि श्रोडिंगर समीकरण के रूप में क्या जाना जाएगा - एक आंशिक अंतर समीकरण जो बताता है कि क्वांटम सिस्टम की क्वांटम स्थिति समय के साथ कैसे बदल जाती है - उन्होंने एक निश्चित स्थिति में इलेक्ट्रॉन खोजने की संभावना का वर्णन करने के लिए गणितीय समीकरणों का भी इस्तेमाल किया। ।
यह इस बात का आधार बन गया कि इलेक्ट्रॉन क्लाउड (या क्वांटम मैकेनिकल) मॉडल के रूप में क्या जाना जाता है, साथ ही साथ श्रोडिंगर समीकरण भी। क्वांटम सिद्धांत के आधार पर, जिसमें कहा गया है कि सभी मामलों में एक तरंग फ़ंक्शन के साथ जुड़े गुण हैं, इलेक्ट्रॉन क्लाउड मॉडल बोहर मॉडल से अलग है कि यह एक इलेक्ट्रॉन के सटीक मार्ग को परिभाषित नहीं करता है।
इसके बजाय, यह संभावनाओं के एक समारोह के आधार पर इलेक्ट्रॉन के स्थान की संभावित स्थिति की भविष्यवाणी करता है। संभाव्यता फ़ंक्शन मूल रूप से एक क्लाउड-जैसे क्षेत्र का वर्णन करता है जहां इलेक्ट्रॉन पाए जाने की संभावना है, इसलिए नाम। जहां बादल सबसे घना है, वहां इलेक्ट्रॉन मिलने की संभावना सबसे बड़ी है; और जहां इलेक्ट्रॉन होने की संभावना कम होती है, वहां बादल कम घने होते हैं।
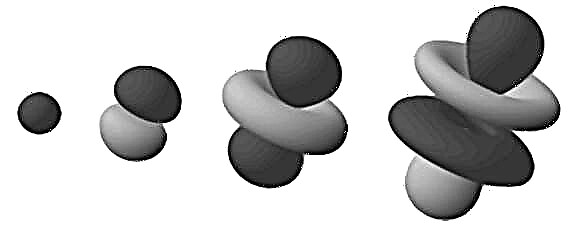
इन घने क्षेत्रों को "इलेक्ट्रॉन ऑर्बिटल्स" के रूप में जाना जाता है, क्योंकि वे सबसे अधिक संभावना वाले स्थान हैं जहां एक परिक्रमा इलेक्ट्रॉन मिलेगा। इस "क्लाउड" मॉडल को 3-आयामी स्थान में विस्तारित करते हुए, हम एक बारबेल या फूल के आकार का परमाणु देखते हैं (जैसा कि शीर्ष पर छवि में है)। यहाँ, ब्रांचिंग क्षेत्र वे हैं जहाँ हम इलेक्ट्रॉनों को खोजने की सबसे अधिक संभावना रखते हैं।
श्रोडिंगर के काम के लिए धन्यवाद, वैज्ञानिकों ने यह समझना शुरू कर दिया कि क्वांटम यांत्रिकी के दायरे में, एक ही समय में एक इलेक्ट्रॉन की सटीक स्थिति और गति को जानना असंभव था। भले ही पर्यवेक्षक किसी कण के बारे में शुरू में जानता हो, वे संभावनाओं के संदर्भ में केवल इसके सफल स्थान या गति का अनुमान लगा सकते हैं।
किसी भी समय वे एक का पता लगाने में सक्षम नहीं होंगे। वास्तव में, वे एक कण की गति के बारे में जितना अधिक जानते हैं, उतना ही कम वे इसके स्थान के बारे में जानेंगे, और इसके विपरीत। इसे ही आज "अनिश्चितता सिद्धांत" के रूप में जाना जाता है।
ध्यान दें कि पिछले पैराग्राफ में उल्लिखित ऑर्बिटल्स एक हाइड्रोजन परमाणु (यानी सिर्फ एक इलेक्ट्रॉन के साथ) द्वारा बनाए गए हैं। जब अधिक इलेक्ट्रॉनों वाले परमाणुओं के साथ काम करते हैं, तो इलेक्ट्रॉन कक्षीय क्षेत्र समान रूप से एक गोलाकार फ़ज़ी बॉल में फैल जाते हैं। यह वह जगह है जहां 'इलेक्ट्रॉन क्लाउड' शब्द सबसे उपयुक्त है।
इस योगदान को सार्वभौमिक रूप से 20 वीं शताब्दी के लागत महत्वपूर्ण योगदानों में से एक के रूप में मान्यता प्राप्त थी, और एक जिसने भौतिकी, क्वांटम यांत्रिकी और वास्तव में सभी विज्ञानों के क्षेत्र में एक क्रांति को जन्म दिया। थेनफोर्थ, वैज्ञानिक अब ब्रह्मांड में काम नहीं कर रहे थे जो समय और स्थान के निरपेक्षता की विशेषता थी, लेकिन क्वांटम अनिश्चितताओं और समय-स्थान सापेक्षता में!
हमने अंतरिक्ष पत्रिका में परमाणुओं और परमाणु मॉडल के बारे में कई दिलचस्प लेख लिखे हैं। यहाँ जॉन डाल्टन का परमाणु मॉडल क्या है ?, बेर का हलवा मॉडल क्या है ?, बोह्र का परमाणु मॉडल क्या है ?, कौन डेमोक्रिटस थे ?, और एक परमाणु के हिस्से क्या हैं?
अधिक जानकारी के लिए, क्वांटम यांत्रिकी की जाँच करना सुनिश्चित करें? लाइव साइंस से।
एस्ट्रोनॉमी कास्ट में एपिसोड 130, रेडियो एस्ट्रोनॉमी, एपिसोड 138: क्वांटम मैकेनिक्स, और एपिसोड 252 जैसे विषय पर भी एपिसोड है: हाइजेनबर्ग अनिश्चितता सिद्धांत